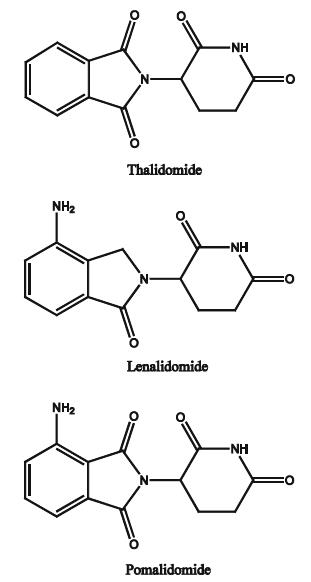
Posteriormente se inició su comercialización para el tratamiento de náuseas y vómitos durante el embarazo. A los pocos años se comenzaron a registrar casos aislados de focomegalia. Su acción teratogénica (malformaciones congénitas) en recién nacidos fue la razón por la que a los años se retiraron aquellos fármacos que contenían talidomida.
No se conocen las cifras a nivel mundial de las personas afectadas con exactitud, pero se ha estimado que existen más de 10000 personas afectadas en todo el mundo.
En la actualidad se están realizando nuevos estudios con este fármaco y sus derivados buscando nuevas aplicaciones. El descubrimiento de sus propiedades antiangiogénicas, antiinflamatorias e inmunomoduladora ha hecho que esta droga comience a utilizarse como terapia de segunda elección en algunas enfermedades de difícil tratamiento, como la leucemia, la lepra o la enfermedad de Behçet.
Este trabajo fue planteado debido al gran estigma social que tiene este fármaco. Sobre todo, en la sociedad española, es un tema muy controvertido debido a su retirada tardía del mercado y el alto número de casos que hubieron en todo ese periodo en el que se comercializaron medicamentos con este fármaco.
Este trabajo de revisión bibliográfica trata la existencia de las nuevas aplicaciones de la talidomida y la puesta en marcha de nuevos estudios que corroboren la eficacia de este fármaco en diversas aplicaciones, haciendo posible que se reinstalen estos fármacos en el mercado, ya que los nuevos estudios están resultando esperanzadores.
En concreto, se ha extendido mucho el uso de la Talidomida y sus derivados en el mieloma múltiple y eritema nudoso leproso, además de otras aplicaciones en dermatología.
Este trabajo se centró en concreto en el estudio de este fármaco como terapia alternativa en el tratamiento del mieloma múltiple.
El mieloma múltiple es una neoplasia hematológica que genera una anormal proliferación de células plasmáticas en la médula ósea, ello provoca un aumento de la liberación de inmunoglobulinas en sangre. La complicación más grave y frecuente de esta patología es la insuficiencia renal producida por la excesiva liberación de las cadenas kappa de las inmunoglobulinas por la sobrecarga de sus receptores en el riñón. Todo esto lleva al fracaso renal agudo, en los cuales gran parte de los pacientes necesitan una terapia renal sustitutiva.
La incidencia de esta enfermedad es de 3-5 nuevos casos por cada 100000 habitantes. La edad media de diagnóstico es de 65 años.
Metodología
Para la recopilación de datos acerca de la Talidomida y sus nuevos usos, se realizó una búsqueda inicial en distintos buscadores bibliográficos: PubMed, Medline, Dialnet, Google académico, EBSCO, Food and Drug Administration.
Se buscaron artículos en castellano y/o inglés, seleccionando aquellas aplicaciones no referidas en la ficha técnica o poco conocidas de este fármaco que existen en la actualidad, con alto potencial en sus posibles aplicaciones como alternativa a tratamientos clásicos y distintas terapias que no han sido efectivas hasta el momento.
También se realizaron búsquedas de los distintos derivados de la talidomida, como la Lenalidomida o Pomalidomide, ya que estos fármacos se están empleando en nuevas terapias y están adquiriendo relevancia en la actualidad.
La búsqueda se acotó a aquellos artículos que no superasen los 5 años de antigüedad, y se centró básicamente en aquellos estudios con resultados relevantes y que aspiran potencialmente a constituir nuevas terapias en un futuro para enfermedades con dificultad de tratamiento.
Los artículos que fueron seleccionados trataban tanto de estudios clínicos, como revisiones bibliográficas, casos clínicos y artículos de investigación, para tratar de incluir la mayor evidencia del uso de la Talidomida en distintas patologías.
 Resultados y discusión
Resultados y discusión
Recientemente en EEUU y en Europa se ha aprobado el uso de lenalidomida y pomalidomida para el tratamiento de mieloma múltiple recurrente asociado a dexametasona, en concreto, en España ha sido aprobada en este mismo año. La clave de su eficacia reside en que este grupo de fármacos son inmunomoduladores, antiangiogénico, antineoplásico y evita la proliferación celular.
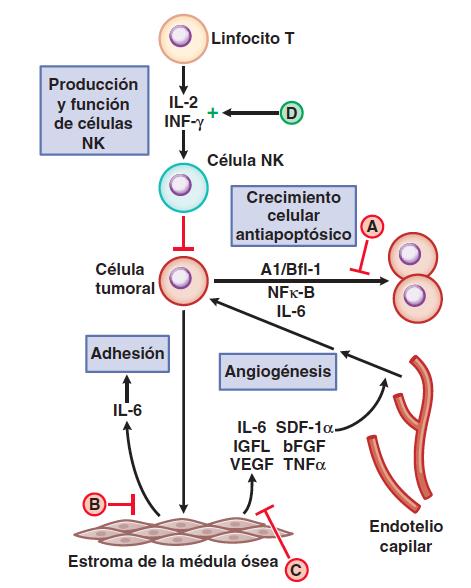 En concreto, la lenalidomida impide la proliferación debido a que produce la apoptosis en células tumorales. No se conoce muy bien el mecanismo aunque se presupone el esquema presentado a continuación. Estos fármacos son inmunomoduladores porque inhiben las citoquinas inflamatorias, IL-1, IL-6, IL-12, TNF alfa. Inhiben de manera indirecta el crecimiento de las células tumorales al eliminar la interacción celular con moléculas de adhesión, inhibición de la liberación y producción de IL-6 y TNF alfa lo que conlleva a su efecto antiangogiogénico. Además, incrementa la producción de NK y linfocitos T, que eliminan las moléculas tumorales.
En concreto, la lenalidomida impide la proliferación debido a que produce la apoptosis en células tumorales. No se conoce muy bien el mecanismo aunque se presupone el esquema presentado a continuación. Estos fármacos son inmunomoduladores porque inhiben las citoquinas inflamatorias, IL-1, IL-6, IL-12, TNF alfa. Inhiben de manera indirecta el crecimiento de las células tumorales al eliminar la interacción celular con moléculas de adhesión, inhibición de la liberación y producción de IL-6 y TNF alfa lo que conlleva a su efecto antiangogiogénico. Además, incrementa la producción de NK y linfocitos T, que eliminan las moléculas tumorales.
La eliminación del fármaco se realiza por vía renal en un 65-70%.
La eficacia clínica de la Lenalidomida asociada a Dexametasona ha sido testada gracias a dos ensayos aleatorios doble ciego. Estos ensayos mostraron una elevada mejoría con respecto al tiempo medio de progresión de la enfermedad. En concreto, el grupo control tuvo un tiempo medio de 4,5 meses, frente a 13,4 meses de aquellos pacientes sometidos al tratamiento.
El mecanismo de acción de la Pomalidomida es similar a este en cuanto a los efectos producidos.
Los principales efectos adversos de la Talidomida y sus derivados son la producción de neutropenia, trombocitopenia y anemia en un porcentaje muy elevado.
La evidencia muestra que la talidomida y sus derivados son fármacos que pueden mejorar el devenir del mieloma múltiple recurrente, que ha sido tratado anteriormente con otra medicación sin dar resultados positivos. Si que es cierto que estos fármacos presentan con frecuencia efectos adversos que deben ser mencionados, pero por otro lado, es la única alternativa a los fármacos anteriores ineficaces.
Los estudios en pacientes con mieloma múltiple muestran una significativa mejora en todos los parámetros de la enfermedad debido a la acción inmunomoduladora del fármaco.
Estos estudios abren una nueva vía y esperanza para aquellas personas que padecen enfermedades raras, ya que este nuevo grupo de fármacos inmunomoduladores pueden tener diversas aplicaciones debido a que actúan sobre intermediarios inflamatorios muy presentes en diferentes patologías.
Conclusión
La Talidomida ha sido un fármaco empleado durante muchos años por sus propiedades sedantes, hipnóticas y anticinetósicas. Posteriormente su uso descendió por la aparición de efectos adversos en mujeres embarazadas, debido a la falta de ensayos clínicos. En estudios recientes se ha demostrado su efectividad en otras áreas, gracias a sus acciones antiangiogénicas, inmunomoduladores y antiinflamatorias, pudiendo considerarse una valiosa herramienta contra diversas enfermedades de origen inflamatorio.
Aun así, el uso de la talidomida debe realizarse con precaución debido a los graves efectos adversos que presenta, teniendo una consideración especial en pacientes que presentan problemas renales y mujeres en edad fértil.
La investigación sobre el origen de diversas enfermedades de base inflamatoria, así como todos los mecanismos asociados a la patología, y el conocimiento del mecanismo de acción de diversos fármacos, hace posible la atribución de nuevas indicaciones a diversos fármacos. Esto permite la ampliación de las posibilidades de tratamiento en enfermedades donde ha fracasado el régimen terapéutico convencional y dando alternativa a los pacientes, como es el caso del mieloma múltiple recurrente.
Bibliografía
1. Vega J, Goecke H, Rodgríguez M, Vergara M. Uso de talidomida en sangrado recurrente por angiodisplasias gastrointestinales. Medicina Chile, 2011,139; 909-913.
2. Ávila CabreraI O, Espinosa Martínez E, Hernández Padrón C, Lisset Izquierdo Cano, Ramón Rodríguez L, Espinosa Estrada E. Treatment of chronic idiopathic myelofibrosis with talidomide low doses. Revista Cubana de Hematología, Inmunología y Hemoterapia, 2010; 26(2) 57-61.
3. Garderet L, Iacobelli S, Moreau P, et al. Superiority of the triple combination of bortezomib-thalidomide-dexamethasone over the dual combination of thalidomide-dexamethasone in patients with multiple myeloma progressing or relapsing after autologous transplantation: The MMVAR/IFM 2005-04 randomized phase III trial from the chronic leukemia working party of the European Group for Blood and Marrow Transplantation. J Clin Oncol 2012; 14-15
4. Bowcock SJ, Patrick HE. Lenalidomide to control gastrointestinal bleeding in hereditary haemorrhagic telangiectasia: potential implications for angiodisplasias? Br J Haematol 2009; 146: 2202.
5. Jiménez Lozano I, Juárez Jiménez J.C. Revisión de la evidencia de talidomida y lenalidomida en diferentes enfermedades hematológicas: leucemia linfocítica crónica, amiloidosis primaria, mielofibrosis y síndromde mielodisplásico. Farmacia Hospitalaria 2013; 37 (4): 322-33.
6. Kay NE, Shanafelt TD, Call TG, Wu W, Laplant BR. N9986: A phase II trial of thalidomide in patients with relapsed chronic lymphocytic leukemia. Leuk Lymphoma 2009;50(4):588-92.
7. Furman R, Leonard J, Allen S, Coleman M, Rosenthal T, Gabrilove JL. Thalidomide alone or in combination with fludarabine are effective treatments for patients with fludarabine relapsed and refractory CLL. J Clin Oncol 2005;23:595
8. Chanan-Khan A, Miller KC, Musial L, Lawrence D, Padmanabhan S, Takeshita K, et al. Clinical efficacy of lenalidomide in patients with relapsed or refractory chronic lymphocytic leukemia: results of a phase II study. J Clin Oncol 2006;24:5343-9.
9. Ferrajoli A, Lee BN, Schlette EJ, O’Brien SM, Gao H, Wen S, et al. Lenalidomide induces complete and partial remissions in patients with relapsed and refractory chronic lymphocytic leukemia. Blood 2008;111(11):5291-7.
10. Brunton L, Chabner B, Knollman B. Goodman y Gilman. Las bases farmacológicas de la terapéutica. Mac Graw Hill. Méjico 2012
11. Papaseit E, García-Algar O, Farré M. Talidomida: una historia inacabada. Anales de pediatría 2013;78 Vol 5: 283-287
12. Cantín Lahoz V, Rojo Zulaica E, Vecino Soler A, Marcén Letosa M, Aznar Buil B. El fracaso renal agudo por mieloma múltiple: cuidados de los pacientes en una unidad de hemodiálisis 2014. Vol 17;2
13. Ramos Ortega F (05/11/2015) https://www.aecc.es/SOBREELCANCER/CANCERPORLOCALIZACION/MIELOMAMULTIPLE/Paginas/incidencia.aspx