Introducción
El cáncer es la segunda causa de muerte a escala mundial. Es una enfermedad en la cual las células del organismo empiezan a adoptar una estructura diferente a las células originales maduras, éstas se multiplican de forma muy rápida y autónoma, pudiendo llegar a otros tejidos y órganos (metástasis). Este tipo de enfermedad no se restringe únicamente a una zona del organismo, sino que puede aparecer en cualquier zona del cuerpo.
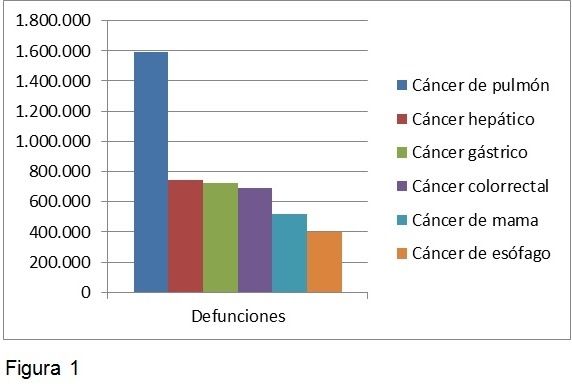
El último estudio de la Organización Mundial de la Salud (OMS) sobre el cáncer mundial fue en 2012. Se registraron 8,2 millones de casos nuevos y se estima que subirá a 22 millones anuales en las próximas dos décadas. Los tipos de tumores que más muertes causan son: cáncer de pulmón, hígado, estómago, colon y mama (figura 1).
Los factores de riesgo responsables del 30% de las muertes por cáncer son: índice de masa corporal elevado, ingesta reducida de frutas y verduras, falta de actividad física, consumo de tabaco (el consumo de tabaco es el responsable del 20% de las muertes mundiales por cáncer en general y del 70% de las muertes mundiales por cáncer de pulmón) y consumo de alcohol.
La mortalidad por cáncer se puede reducir si se detectan en una fase temprana de la enfermedad. La detección a tiempo consiste en un diagnóstico temprano (se basa en conocer los signos y síntomas de la enfermedad), y en hacer un cribado, que son pruebas de detección cuando el paciente aún es asintomático. Hoy en día el tratamiento del cáncer es muy variado, depende del tipo de cáncer a tratar, de los efectos secundarios, de las preferencias del paciente y de su estado de salud en general. Entre los tratamientos disponibles, se pueden utilizar en monoterapia o terapia combinada, y se encuentran la quimioterapia, radioterapia, tratamientos dirigidos, inmunoterapia, y la cirugía; este último es el tratamiento más antiguo contra el cáncer.
A día de hoy existe una nueva promesa para el tratamiento del cáncer, un nuevo fármaco para la inmunoterapia: pembrolizumab.
Material y métodos
Se realizó una revisión sobre la última actualización de pembrolizumbab. Para la obtención de los artículos se emplearon dos fuentes documentales. Se realizó una búsqueda bibliográfica de los dos últimos años en PubMed utilizando las siguientes palabras claves: «Pembrolizumab», «MK-3475», «cáncer», «immunotherapy» y «review». Los resultados encontrados son 12 artículos de los cuales seleccionamos 3, ya que los demás no trataban sobre pembrolizumab. También se consultó una página web especializada en la materia –European Society for medical oncology (ESMO)–, con el término «Pembrolizumab».
Innovación terapéutica
Los tres pilares en los que se basaba el tratamiento del cáncer han sido la cirugía, la quimioterapia y la radioterapia. Con estas técnicas se han obtenido grandes resultados, pero hoy en día algunos tumores se hacen resistentes a estos tratamientos. Una nueva esperanza, que potencia las defensas del organismo sin atacar directamente el tumor, es la inmunoterapia. Es una de las vías más prometedoras del tratamiento del cáncer en los próximos 10 años.
Pembrolizumab es un nuevo tratamiento del cáncer basado en la técnica de la inmunoterapia. Es un anticuerpo monoclonal humanizado que se une al receptor PD-1 de los linfocitos T, bloqueando la unión de los ligandos PD-1 de las células tumorales, evitando el tumor del organismo.
 ¿Por qué es una nueva esperanza?
¿Por qué es una nueva esperanza?
Los linfocitos T contienen en su superficie receptores de la superfamilia de las inmunoglobulinas como la PD-1 (program death). Estas moléculas tienen como objetivo detectar células extrañas al organismo (células tumorales) y destruirlas.
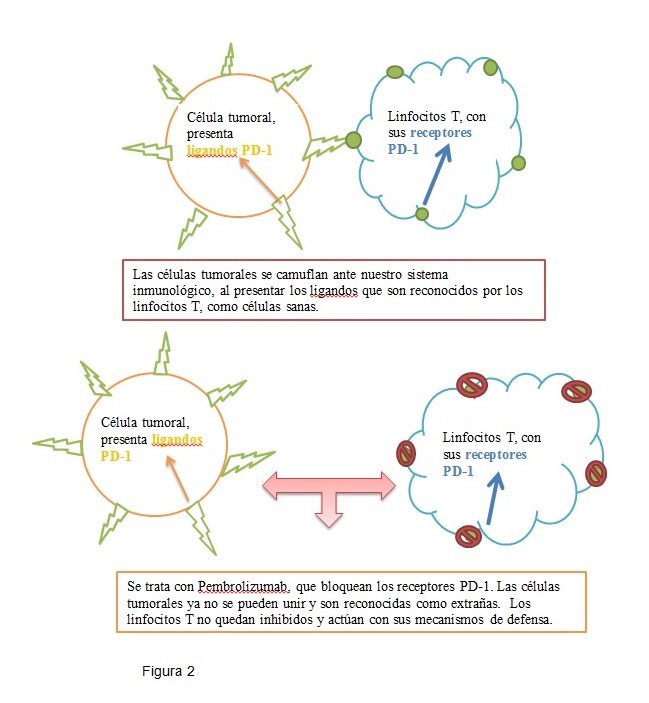
En teoría, las proteínas PD-L1 de las células, son la contraseña para indicar a los linfocitos T que no son cancerígenas, por lo que no debe atacarlas. El problema surge cuando las células tumorales se camuflan como células sanas al expresar en su superficie las proteínas PD-L1, por lo que los linfocitos quedan inhibidos (debido a la unión de las proteínas PD-L1 de las células tumorales al receptor PD-1 de los linfocitos T), frenan la respuesta inmunitaria y las células tumorales pueden seguir multiplicándose e invadiendo el organismo.
Es aquí donde actúa pembrolizumab, uniéndose a los receptores PD-1 de los linfocitos T, por lo que las células tumorales ya no se pueden unir y no pasan desapercibidas ante el sistema inmunitario (figura 2).
Eficacia y selectividad de pembrolizumab
Pembrolizumab se ha estudiado para diferentes tumores y se han obtenido resultados prometedores para el cáncer de pulmón de células no pequeñas (NSCLC), melanoma, cáncer gástrico.
Cáncer de pulmon no microcítico (CPNM) o células no pequeñas (NSCLC)
Alrededor del 85% de los tumores de pulmón son no microcíticos. De este tipo de cáncer, hay tres subtipos: carcinoma de células escamosas, carcinoma de células grandes y adenocarcinoma. Las células de estos tipos de tumores difieren entre sí, pero son agrupados en un conjunto, porque el tratamiento y pronóstico es similar.
El anticuerpo PD-1 (pembrolizumab) ha demostrado una actividad antitumoral duradera y de toxicidad aceptable en pacientes con este tipo de cáncer avanzado (CPNM).
Mediante un estudio de 282 pacientes, durante un seguimiento de 5 meses, se ha observado la correlación entre la expresión del tumor (PD-L1) y la actividad antitumoral de pembrolizumab.
Melanoma avanzado
Para comprobar la eficacia y seguridad de pembrolizumab en pacientes con melanoma avanzado se hizo un estudio en 244 pacientes, que se dividieron en dos de manera aleatoria, cada grupo con una dosis diferente (2 mg/kg o 10 mg/kg cada 3 semanas). El seguimiento fue de aproximadamente 35 semanas.
En general, ambas dosis eran eficaces y con una seguridad similar, por lo que la dosis recomendada fue de 2 mg/kg cada tres semanas.
Pembrolizumab (2 mg/kg/3 semanas) fue aprobado por la Food and Drug Administration de EE.UU. (FDA) el 4 de septiembre 2014 para el tratamiento de los pacientes con melanoma avanzado o que no respondan a otros tratamientos (ipilimumab y fármacos inhibidores del gen BRAF).
Pembrolizumab es el sexto nuevo tratamiento del melanoma aprobado desde 2011.
Cáncer gástrico
Se estudió la seguridad, tolerabilidad y actividad antitumoral de pembrolizumab en 162 pacientes con cáncer gástrico, de los cuales 65 eran PD-L1 positivos. La duración del seguimiento fue de aproximadamente 6 meses. Se obtuvieron resultados en los cuales se afirmaba la relación de la expresión de PD-L1 y la actividad antitumoral de pembrolizumab.
Resultados
En la actualidad, el tratamiento con pembrolizumab sóolo está aprobado para pacientes con melanoma avanzado que hayan sido tratados con ipilimumab. Se ha comprobado la eficacia en pacientes con este tipo de cáncer. ocasionando, en un 24% de los pacientes, una disminución de los tumores con indiferencia de la dosis. Es un tratamiento tolerado; los efectos adversos más comunes son hepatitis, colitis, problemas del tiroides, prurito, náuseas y fatiga, diarrea y estreñimiento. Pembrolizumab, al actuar en el funcionamiento del sistema inmunitario, puede producir reacciones adversas en diferentes partes del organismo, necesitando estos síntomas su propio tratamiento o incluso la retirada del tratamiento antitumoral.
Conclusión
En vista de la información revisada, pembrolizumab a una dosis de 2 mg/kg cada 3 semanas puede ser un tratamiento eficaz. Hoy en día sólo se benefician de este medicamento los pacientes con melanoma avanzado, aunque los estudios de investigación en cáncer avanzado de pulmón de células no pequeñas y cáncer gástrico también muestran una actividad prometedora, evitando la quimioterapia citotóxica. Por lo que el tratamiento con Ac monoclonales es una nueva esperanza para numerosas enfermedades.
Bibliografía
1. Robert C, Ribas A, Wolchok JD, Hodi FS, Hamid O, Kefford R et al. Anti-programmed-death-receptor-1 treatment with pembrolizumab in ipilimumab-refractory advanced melanoma: a randomised dose-comparison cohort of a phase 1 trial. Lancet. 2014 Sep 20; 384(9948):1109-17. [PubMed]
2. Weber JS, Daud A, Joshua AM, Hodi FS, Kefford RF, Wolchok JD, et al. Pembrolizumab (pembro; MK-3475) and correlation with programmed death ligand 1 (PD-L1) expression in a pooled analysis of patients with advanced non-smal cell lung carcinoma (NSCLC). Esmo. 2014 sep 29.
3. Kefford R, Ribas A, Hamid O, Robert C, Daud A, Wolchok JD, et al. Clinical efficacy and correlation with tumor PD-L1 expression in patients with melanoma treated with the anti-PD-1 monoclonal antibody MK-3475. J Clin Oncol 32:5s. 2014 (abstr 3005).